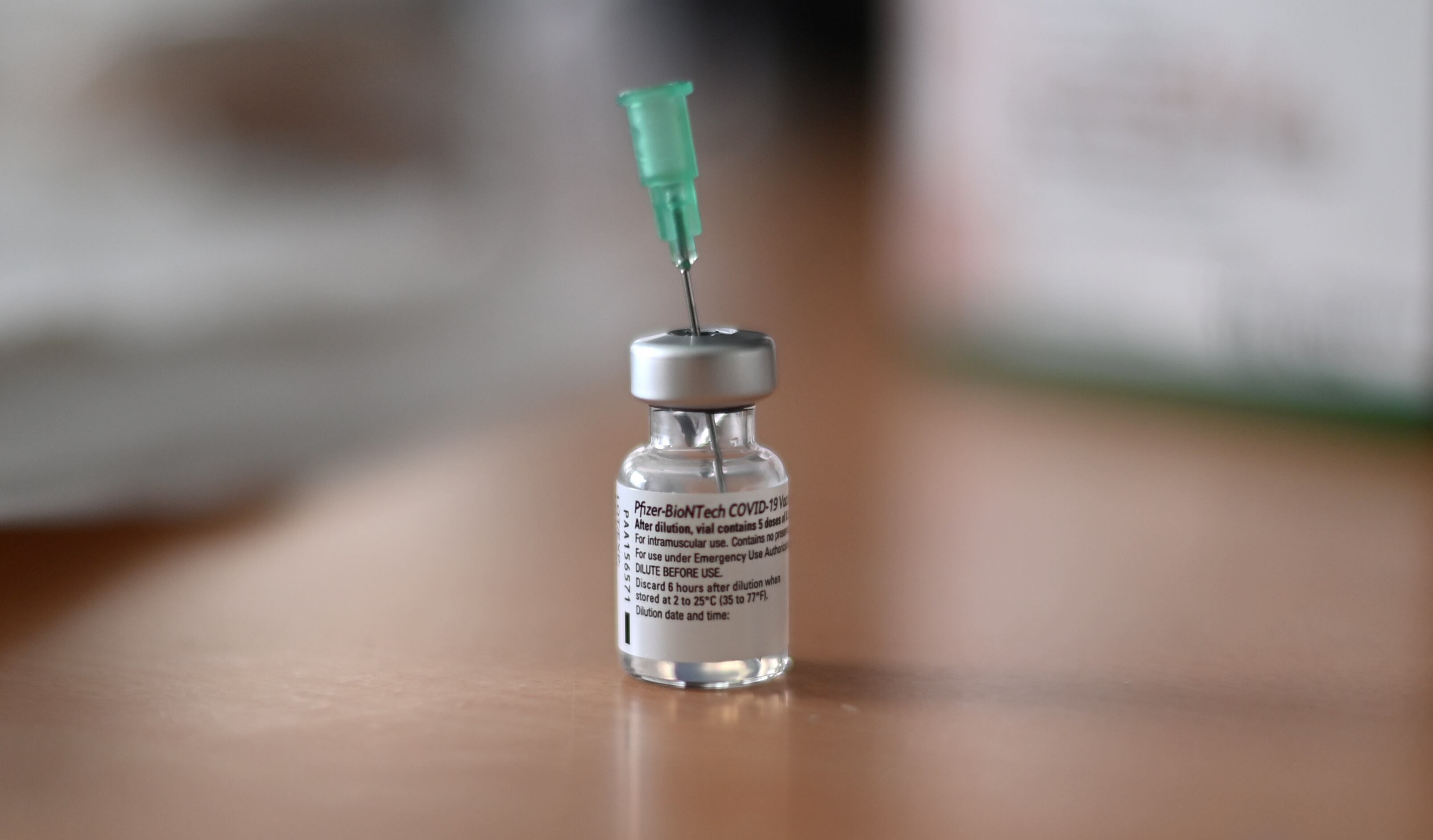
Debido al interés de clínicas y farmacias privadas por comenzar los procesos para vender vacunas contra la covid-19 en Costa Rica, el Ministerio de Salud emitió este martes los requisitos para realizar dicho trámite.
Por medio de la resolución MS-DM-RM-0933-2021, la cartera pretende “dejar totalmente claro al sector empresarial” los pasos requeridos para obtener la autorización de uso e importación de estos fármacos.
Sin embargo, el Ministerio advierte que esto se podrá llevar a cabo una vez que los desarrolladores de vacunas cuenten con las posibilidades de colocar su producto en el sector privado.
El documento detalla que “permitir la venta de la vacuna contra la covid-19 para el mercado privado garantiza el acceso a la salud a mayor cantidad de personas y alcanzar la inmunidad de rebaño en forma más acelerada”.
Además, subraya que la autorización estará vigente mientras se mantenga el estado de emergencia nacional.
Documentación
La institución explicó que el trámite se realizaría ante la Dirección de Regulación de Productos de Interés Sanitario, donde se gestiona la solicitud y la demás información requerida, como certificados de buenas prácticas y detalles del etiquetado.
También se debe entregar la documentación para la comprobación respectiva de los parámetros de calidad, seguridad y eficacia del producto; contar con aprobación de agencia regulatoria estricta y/o precalificación de Organización Mundial de la Salud (OMS) y una eficacia vacunal de al menos un 60%.
De igual forma, una vez que se cuente con las dosis en el país para su venta y/o colocación, se debe coordinar el reporte respectivo del proceso de vacunación y el seguimiento post vacunación de eventos supuestamente atribuibles a vacunación e inmunización.
Asimismo, los sitios autorizados deben asegurar de que la vacuna se distribuya con el etiquetado aprobado y que se mantenga el almacenamiento y la cadena de frío adecuados hasta que se entreguen en los lugares de vacunación.
Fiscalización
Salud indicó que el representante legal debe presentar Informes de Seguridad de forma mensual, dentro de los 15 días posteriores al último día de un mes, comenzando después del primer mes calendario completo posterior a la autorización.
También ordenó que los entidades autorizadas deben mantener registros con respecto a la liberación de la vacuna para su distribución (es decir, números de lote, cantidad, fecha de liberación).
Además, la Dirección de Regulación de Productos de Interés Sanitario podrá solicitar al representante legal y sitios autorizados cualquier información que considere pertinente en relación con la vacuna autorizada.
Estos son otros de los requisitos que deberán cumplir los proveedores de la vacunación:
- Garantizar que la vacunación se realice en establecimientos habilitados para prestar el servicio de vacunación, o que tenga el servicio de vacunación temporal autorizado por el área rectora de salud del Ministerio de Salud.
- Garantizar el cumplimiento en relación con las contraindicaciones, precauciones y advertencias, reacciones adversas, interacciones, vía de administración y dosificación autorizada para la vacuna
- Proporcionar información a las personas sobre los posibles efectos adversos asociados a la vacuna que reciban, proporcionar un carné de vacunación y la información necesaria para recibir su segunda dosis.
- Garantizar el registro en la plataforma SINOVAC.
Por último, Salud indicó que la autorización de comercialización es un requisito previo para la importación de las vacunas, porque su importación debe gestionarse a través del Sistema de Ventanilla Única de Comercio Exterior (Sivuce) de la Promotora del Comercio Exterior de Costa Rica (Procomer).
“Una vez presentada la solicitud de autorización completa, la Administración cuenta con un plazo de 10 días para resolver”, finaliza el documento firmado por el ministro de Salud, Daniel Salas.
