La falta de información sobre la salida de pacientes hemofílicos de un hospital público a una empresa privada para probar un nuevo medicamento le ocasionó a la Caja Costarricense de Seguro Social (CCSS) pérdidas superiores a los $2,2 millones en un año.
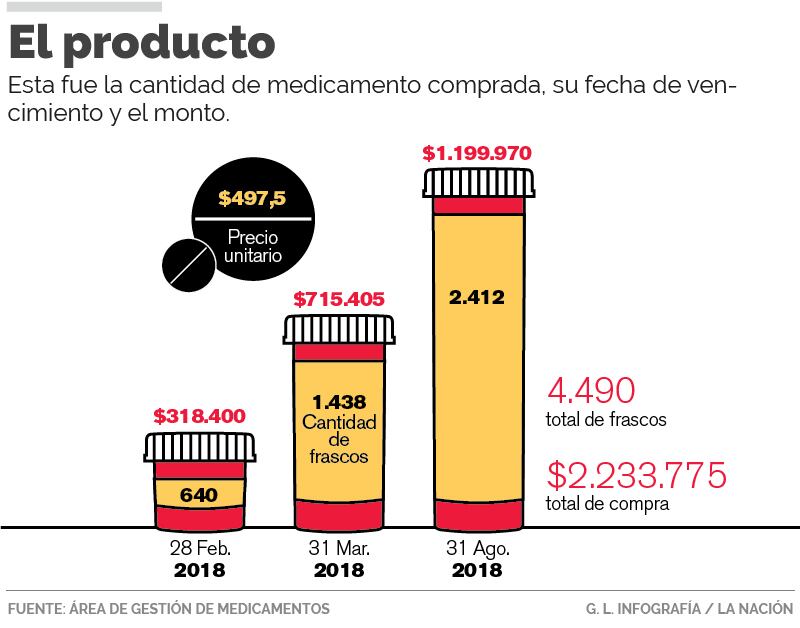
Esa fue la cantidad de dinero que invirtió la institución en la compra de un factor de coagulación anti-inhibidor (que facilita la coagulación sanguínea), conocido como Feiba, considerado uno de los medicamentos más caros adquiridos anualmente por la CCSS.
Por cada frasco del producto la Caja invierte $497,5 y estas personas llegan a consumir varios en un mes.
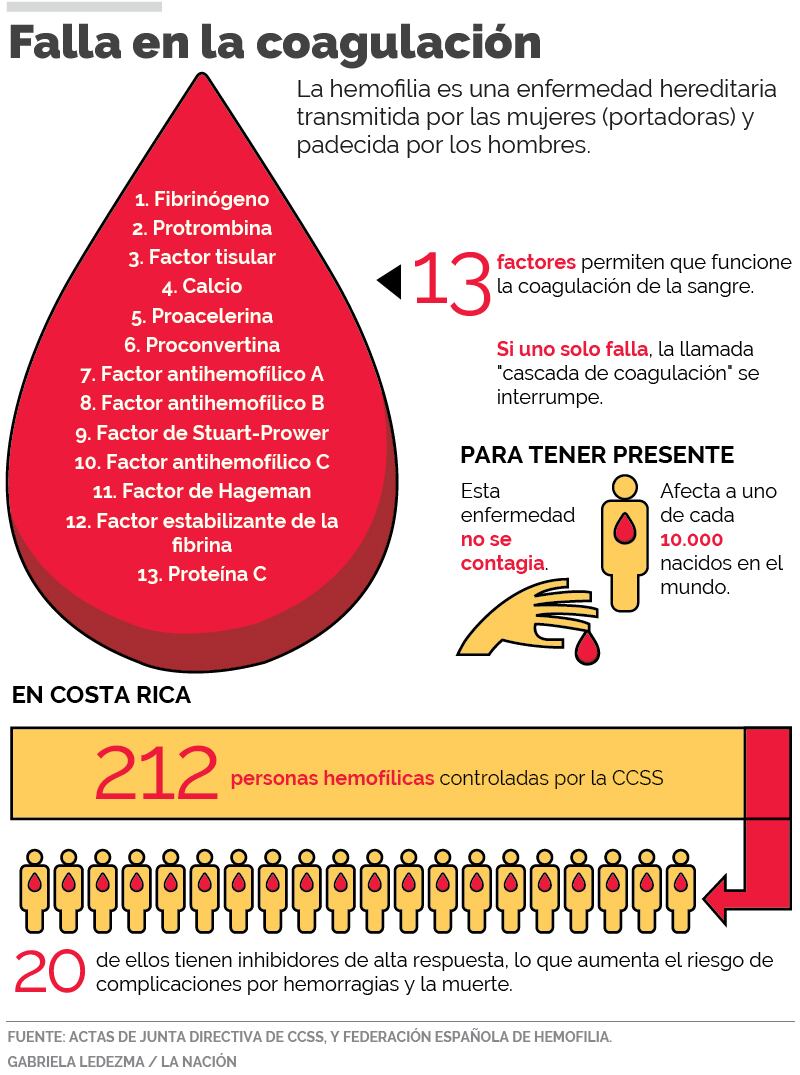
La hemofilia es una enfermedad hereditaria, caracterizada por fallos en la coagulación de la sangre. En el mundo, una de cada 10.000 personas la padece.
En los hospitales públicos llevan control 212 hemofílicos. De ese grupo, hay 20 personas con "inhibidores de alta respuesta" o anticuerpos capaces de interferir en la coagulación cuando alguien tiene un sangrado.
La CCSS llega a invertir más de $4 millones anuales en la compra de medicamentos para esas 20 personas.
Según la institución, seis de estos pacientes dejaron de usar Feiba para participar en un ensayo clínico con otro producto que está a prueba, pero la información nunca llegó a los responsables de la adquisición de los fármacos, a pesar de que dos de los investigadores que participan en el ensayo clínico son funcionarios del Hospital México, donde se trataba a esos enfermos.
Aunque son pocos, los seis pacientes consumían el 80% del producto y el costo de su tratamiento es uno de los más altos.
Angélica Vargas Camacho, jefa del Área de Medicamentos y Terapéutica Clínica de la CCSS, dijo que estos pacientes "le han generado a la institución un elevado impacto financiero porque (lo que consumen) son productos de alto costo".
"Son pacientes que sangran y cuando tienen inhibidores sangran más y tienen más complicaciones producto de su enfermedad. Se les da un medicamento que previene el sangrado. El factor Feiba se incluyó en la Lista Oficial de Medicamentos (LOM) desde el año 2011 con una idea de distribuir recursos y disminuir el consumo del Factor VII que ya se tenía en la Institución", explicó la especialista en la presentación técnica que se le hizo a la Junta Directiva de la CCSS para justificar la firma de un convenio de cooperación.
En los registros de las sesiones del 18, 25 y 29 de enero pasado del máximo órgano de la Caja, dan cuenta del intenso debate que se desarrolló ahí cuando funcionarios de las gerencias Médica y de Logística revelaron la situación a los entonces directores institucionales.
Según se desprende de la revisión de esas actas, la mayoría de pacientes que recibían ese fármaco migraron en circunstancias que que aún se investigan hacia una empresa privada –cuyo nombre no se menciona– que les ofreció probar un nuevo fármaco para controlar su enfermedad.
Ese traslado provocó una caída en el consumo del producto de la CCSS –que ya había sido adquirido previamente–, al punto de registrar disminuciones de un 75% (en el caso del Feiba) y un 90% en otro fármaco, conocido como Factor VII recombinante, entre el 2016 y 2017.
De acuerdo con informes técnicos presentados a la Junta Directiva en enero, y que constan en las actas, el consumo pasó de 538 frascos mensuales a 150 en cuestión de un trimestre, entre el 2017 y 2018.

Fernando Llorca Castro, presidente ejecutivo de la Caja con recargo de la Gerencia Médica, confirmó a este medio que se instruyó ordenar una investigación preliminar sobre este caso.
"La Junta Directiva ratificó el acuerdo y dicha investigación está pronta a terminar", informó Llorca. El acuerdo lo tomó la anterior Junta Directiva, que terminó su periodo el 31 de mayo.
¿Cómo consiguió la empresa privada los nombres de pacientes de la Caja? ¿Quién autorizó dar esos contactos y bajo cuáles condiciones? ¿Fueron los enfermos debidamente informados sobre esta situación? ¿Cuáles son las responsabilidades que se deben establecer tras el impacto económico sufrido por la institución?
Las anteriores son parte de las preguntas que deben ser contestadas.
Por ahora, un informe de la Auditoría Interna de la CCSS –el ASAAI-06-2018, del 5 de febrero anterior–, constató, además, que los estudios clínicos con pacientes hemofílicos "no fueron puestos (sic) del conocimiento de las autoridades institucionales, pese a que dos investigadores fungen como funcionarios del Hospital México".
La Auditoría recomienda, incluso, denunciar penalmente ante el Ministerio Público "lo que en derecho corresponda".
Además, encontró evidencia de la disponibilidad de 4.490 unidades de ese producto con fechas de vencimiento entre febrero y agosto de 2018. Según anota el informe, "el riesgo de vencimiento" se calculaba en más de ¢975 millones.
Donación "en carrera"
El ahora llamado "caso Feiba" llegó a la Junta Directiva de la CCSS como parte de un proceso para autorizar la donación del medicamento a la Federación Mundial de Hemofilia, pues el producto estaba a punto de vencer.
La donación es parte de un convenio y asciende a 3.352 frascos, que representaron una inversión para la CCSS de $1,6 millones. El medicamento fue enviado a Venezuela.
A cambio, la Federación se comprometió a dar cursos de capacitación sobre la enfermedad a funcionarios institucionales. El costo de esa capacitación es el equivalente a 88 frascos de Feiba ($44.000), apuntan las actas de la CCSS.
Según las presentaciones técnicas realizadas en enero a la Junta Directiva por la entonces gerenta de Logística, Dinorah Garro Herrera, y la gerenta médica, María Eugenia Villalta Bonilla, se probaron diferentes medidas para aprovechar el medicamento antes de concluir que la única salida era la donación con carácter humanitario.
Incluso, según consta en actas, hubo reuniones con el proveedor del fármaco para cambiarlo por otro con mayor periodo de vencimiento, y se contactó a organizaciones de salud en el mundo por medio de la Cancillería para informar de que el medicamento estaba a la venta.
No obstante, ninguna de estas opciones fructificó, por lo que se tuvo que recurrir a la donación a la Federación Mundial de Hemofilia.
Uno de los entonces miembros de la Junta Directiva, Rolando Barrantes Muñoz, hace constar en actas "el esfuerzo que han hecho las dos gerencias para salvar un gran error".
Barrantes, quien fuera representante del Estado en esa Junta, recalcó su preocupación por la falta de regulación interna en el tema de la investigación clínica.
Adolfo Gutiérrez, representante patronal ante ese mismo órgano en la anterior Junta, también dejó patente su preocupación sobre este tema.
"En la investigación es importante no solo determinar que hubo seis pacientes que participaron, si no definir cómo se integran esos pacientes a la investigación, cuál fue la información, quién la dio a la farmacéutica, cómo conocen que esos pacientes eran las personas, (...) y por qué la empresa conocía el número de pacientes que consumían los medicamentos en la Caja", dijo Gutiérrez.
El ahora exdirector, consultó sobre la posibilidad de que estos enfermos se "devuelvan" a la Caja si el tratamiento que está a prueba no les funciona.
Para Gutiérrez, según consta en actas, si los pacientes regresan se "estaría produciendo un impacto significativo en el consumo del medicamento".
Marjorie Arias, una de las especialistas que acudieron ante Junta Directiva, aseguró que "una de las contraindicaciones (para los pacientes que participan en el ensayo clínico) es el uso del factor Feiba".
"Los pacientes no se pueden devolver a utilizar ese medicamento. Pueden utilizar el Factor VII que es la otra opción, pero es más costosa para la institución", advirtió Arias.
El auditor de la CCSS, Jorge Arturo Hernández Castañeda, insistió en todas las discusiones sobre este asunto en considerar dentro de la investigación "la responsabilidad de la empresa que condujo (a la Caja) a esa situación para determinar si existe una implicación de carácter legal".
Investigación biomédica en revisión
El presidente ejecutivo de la CCSS, Fernando Llorca, reconoció a sus entonces compañeros directores que todo lo relacionado con la investigación biomédica dentro de la Caja está en revisión.
Según consta en las actas en las que se discutió el caso Feiba, Llorca reconoce que se tiene "una oportunidad para abordar este tema porque lo importante es asegurar que situaciones similares no vuelvan a suceder".
"Se está en ese proceso y con la Gerencia Médica, el Centro de Desarrollo Estratégico e Información en Salud y Seguridad Social (Cendeisss) se ha venido revisando una actualización del reglamento", informó Llorca Castro a la directiva.
Rolando Barrantes fue uno de los directores que, en el momento en que se discutió el caso Feiba, insistió más en responder cuestiones ligadas con la investigación clínica.
"Quién autorizó esa investigación, cómo se seleccionaron los pacientes y si la Caja participó con recursos institucionales. Esas tres preguntas no han tenido respuesta y deben tenerla", sostuvo Barrantes en la discusión.
Para él, también se debe identificar al Comité Ético-Científico involucrado en esa investigación y encontrar el acta del Conis (Consejo Nacional de Investigación en Salud) donde se aprobó ese ensayo con pacientes de la CCSS.