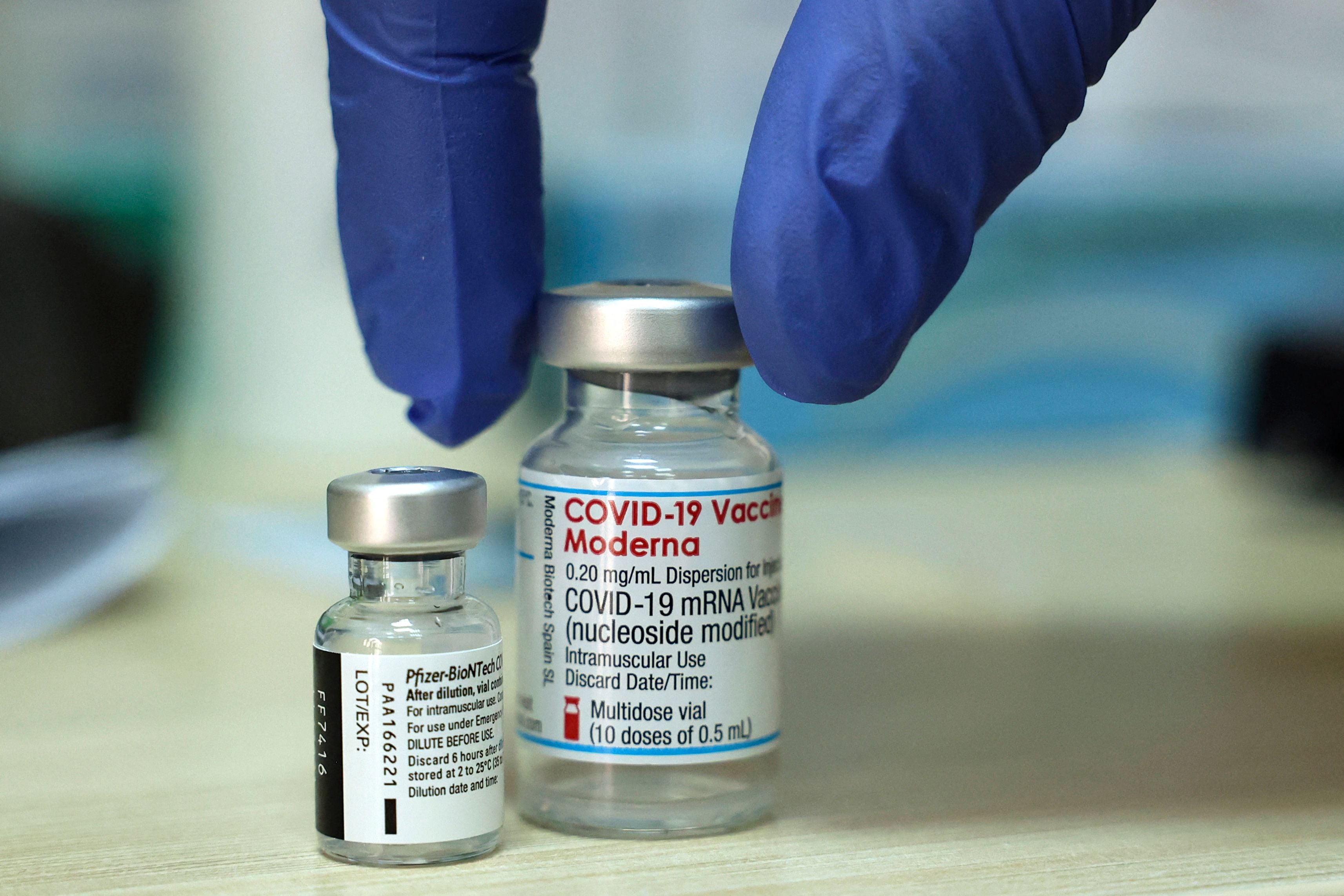
Los vacunados contra la covid-19 que requieran una vacuna de refuerzo pueden recibir una marca distinta a la aplicada en su esquema inicial, según una autorización de emergencia comunicada este miércoles por la Agencia de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés). Esto se conoce como esquema heterólogo.
A través de un comunicado de prensa, el ente regulador informó de que las personas pueden decidir si cambian o no la marca de su esquema inicial. Al ser una agencia estadounidense, las recomendaciones se hacen para las tres vacunas utilizadas en aquella nación: Pfizer y BioNTech, Moderna y Johnson & Johnson.
Las recomendaciones de quiénes podrían recibir la dosis extra varían según la vacuna. Por ejemplo, los que recibieron el producto de Johnson & Johnson (cuyo esquema inicial es unidosis), puede recibir el refuerzo todos los mayores de 18 años. Este se debe aplicar al menos dos meses después de la primera inyección.
Estos usuarios podrán elegir entre una dosis del mismo producto, una de Pfizer o media dosis de Moderna (dado que su refuerzo es de solo la mitad de la sustancia).
En quienes tienen tanto Pfizer como Moderna, la recomendación de booster es para los mayores de 65 años. Las personas entre 18 y 64 podrían recibirlo si tienen condiciones predisponentes para complicarse o fallecer de covid-19 y si son trabajadores de primera línea y, por lo tanto, mayor riesgo de infección y de desarrollar la enfermedad.
En este caso, el refuerzo se aplica seis meses después de la segunda dosis. Estas personas podrán decidir si reciben una dosis de la vacuna ya recibida (o media dosis, en el caso de Moderna) o si cambian a una de Johnson & Johnson o de la otra compañía.
Las vacunas de Pfizer y de Moderna son de una misma tecnología, llamada ARN mensajero, mientras que la de Johnson & Johnson utiliza otra, denominada adenovirus. Esta técnica es la misma usada en la vacuna de AstraZeneca; el fármaco del laboratorio inglés no fue tomado en cuenta para el autorización de la FDA porque este no es utilizado en Estados Unidos, por ello, no se analizó.
Las autoridades consideran que los adolescentes y los adultos de entre 18 y 64 años, que están saludables y que no tienen mayor exposición al virus, de momento no requieren inocularse nuevamente.
“Trabajaremos para analizar la información científica tan pronto como sea posible, para poder analizar los riesgos y beneficios de los booster en otras poblaciones. Planeamos mantener al día a la comunidad de profesionales de salud y del público en general en las próximas semanas”, señaló Peter Marks, director del Centro de Evaluación e Investigación de Biológicos de la FDA.
LEA MÁS: Secuelas de covid-19 obligan a Ileana Balmaceda a dejar proyecto para reestructurar CCSS
En Costa Rica
En nuestro país es poco lo normado sobre dosis adicionales. El viernes pasado se indicó que quienes se habían vacunado con Johnson & Johnson en el extranjero (fármaco que no está disponible en Costa Rica) podrían recibir ambas dosis de la farmacéutica AstraZeneca. Entre el 1.º de marzo y el 31 de julio, 7.542 costarricenses obtuvieron este producto.
Esto no es considerado un refuerzo, dado que es otro esquema completo. La recomendación de la Comisión Nacional de Vacunación y Epidemiología (CNVE) es que esto se realice al menos cuatro semanas después de haber sido inoculado con el producto estadounidense.
Las autoridades costarricenses sí han hablado de dar dosis adicionales para tres poblaciones: los mayores de 58 años, los trabajadores de la primera línea de atención a la pandemia y las personas cuyos sistemas de defensas no funcionan bien y requieren de mayor vacuna para montar su respuesta de defensas, quienes se conocen como inmunocomprometidos. Los inmunosuprimidos, individuos con un menor funcionamiento inmunitario, también están en esta lista.
El 5 de agosto, el Gobierno anunció que negocia con Pfizer más vacunas para los dos primeros grupos. Doce días después, el 17, la Comisión Nacional de Vacunación y Epidemiología (CNVE) informó de que las personas con problemas inmunitarios también recibirían una tercera dosis. Sin embargo, no se precisó cuáles condiciones específicas están incluidas en esta lista.
Para el médico infectólogo Saúl Quirós Cárdenas, el aval de la FDA al esquema heterólogo de vacunas también abre puertas para Costa Rica.
“Esto permitiría arrancar antes la vacunación con tercera dosis para las poblaciones prioritarias que ya había definido la CNVE, dado que no habría necesariamente que esperar al 2022 y se podría colocar tercera dosis tanto de AstraZeneca como de Pfizer”, manifestó.
LEA MÁS: Adolescentes podrán vacunarse contra covid-19 a partir de este lunes 25 de octubre
