Hace cuatro mil millones de años, nuestro planeta era agua y roca estéril. De esto, surgió una química muy complicada, tal vez en un estanque o en una profunda chimenea submarina. Con el tiempo, esa química se envolvió en membranas, se desarrolló una célula primitiva y la vida surgió.
Pero, ¿cómo? Es un problema del huevo o la gallina. Proteínas denominadas enzimas, que ponen en marcha reacciones químicas dentro de las células, se crean a partir de instrucciones en el material genético: el ADN o el ARN. Pero al principio, esas moléculas no existían: para fabricarlas, se necesitan enzimas.
Entonces, ¿qué puso las cosas en marcha?
Una idea que los científicos han barajado mucho tiempo es que el material genético fue lo primero —en forma de una molécula llamada ARN, primo cercano del ADN—. El ARN es versátil: puede catalizar reacciones químicas y almacenar información genética. Así que tal vez en un lago en la superficie de la Tierra, las moléculas se concentraron por evaporación y luego se unieron para formar las primeras cadenas de ARN.
Pero hasta ahora, los científicos no han sido capaces de crear moléculas de ARN en experimentos que imiten las sopas de sustancias químicas simples que habrían existido en la Tierra primitiva.
“Ha habido informes de cómo hacerlo, pero parecen un poco artificiales”, dice Albert Fahrenbach, químico orgánico de la Universidad de Nueva Gales del Sur en Sídney.
Es difícil imaginar que un sistema de cadenas de ARN autorreplicantes pudiera haberse organizado espontáneamente, dice Robert Pascal, químico que trabaja en los orígenes y el surgimiento de la vida en la Universidad de Aix-Marsella en Francia.
Otra opción es que la bioquímica fuera lo primero —evolucionó como geoquímica, fuera de las células—. Las reacciones químicas habrían tenido lugar sin enzimas al principio, muy lentamente. Avanzarían poco a poco porque estaban favorecidas termodinámicamente y, posiblemente, aceleradas por el calor o los metales. Más tarde, se desarrollaron enzimas primitivas, acelerando aún más esa química primordial de la vida.
Con el tiempo la geoquímica se habría vuelto más rápida y elaborada, añadiendo nuevas reacciones. En algún momento, habrían surgido las membranas celulares y un sistema de herencia, en forma de ARN o ADN. La geoquímica se transformaría en bioquímica.
Esta segunda hipótesis carecía de pruebas experimentales clave hasta hace relativamente poco. En los últimos años, científicos han probado en el laboratorio vastas combinaciones de mezclas y condiciones químicas e identificaron formas de replicar reacciones metabólicas básicas de las células —sin enzimas—.
La idea de que la geoquímica precedió a la bioquímica es “realmente poderosa”, afirma Susan Lang, geoquímica del Woods Hole Oceanographic Institution en Massachusetts.
LEA MÁS: Hipótesis sobre origen de la vida emerge en Guanacaste
Orígenes inorgánicos
En 1910, el biólogo Konstantin Sergejewitch Mereschkowsky razonó que las primeras células tuvieron que producir moléculas orgánicas a partir de sustancias inorgánicas: tomar hidrógeno y dióxido de carbono para fabricar moléculas orgánicas como ácidos grasos, azúcares y aminoácidos.
Hace unos 20 años, el microbiólogo evolutivo Bill Martin, de la Universidad de Düsseldorf, en Alemania, y el geoquímico Mike Russell, del Laboratorio de Propulsión a Chorro de la NASA, en California, propusieron que la vida comenzó en un lugar adecuado para estas reacciones críticas: las fuentes hidrotermales de las profundidades marinas.
Dentro de estas fumarolas hidrotermales, el hierro de la roca reacciona con el agua para producir hidrógeno. Y ese hidrógeno podría reaccionar con el CO2 para producir moléculas orgánicas simples fundamentales para la bioquímica celular: el formiato, el acetato y el piruvato.
Guiados por esta idea, en 2010 Lang y su equipo en Woods Hole, trabajando en la Ciudad Perdida, un campo hidrotermal en medio del Océano Atlántico, confirmaron que pequeñas moléculas orgánicas se producen en las fuentes.
LEA MÁS: La vida en la Tierra se originó 220 millones de años antes de lo que se pensaba
Una vía microbiana
Los científicos observaron que los pasos de estas reacciones geoquímicas en las fuentes hidrotermales son idénticos a los de las células microbianas que viven cerca de las fuentes hidrotermales y orgánicas a partir de CO2 e hidrógeno. Esto encaja con la idea de que las vías bioquímicas comenzaron como reacciones geoquímicas y las enzimas evolucionaron más tarde.
Martin y sus colegas demostraron que este conjunto particular de reacciones, conocido como la vía del acetil-CoA, es muy antiguo. Es compartido por dos grupos fundamentales de vida, las bacterias y las arqueas.
Pero las células microbianas actuales necesitan 127 enzimas para producir ese piruvato de tres carbonos. ¿Podrían los científicos replicar esta vía en un laboratorio, sin enzimas, como habría sido en los albores de la vida? Martin y sus colegas demostraron que podían hacerlo.
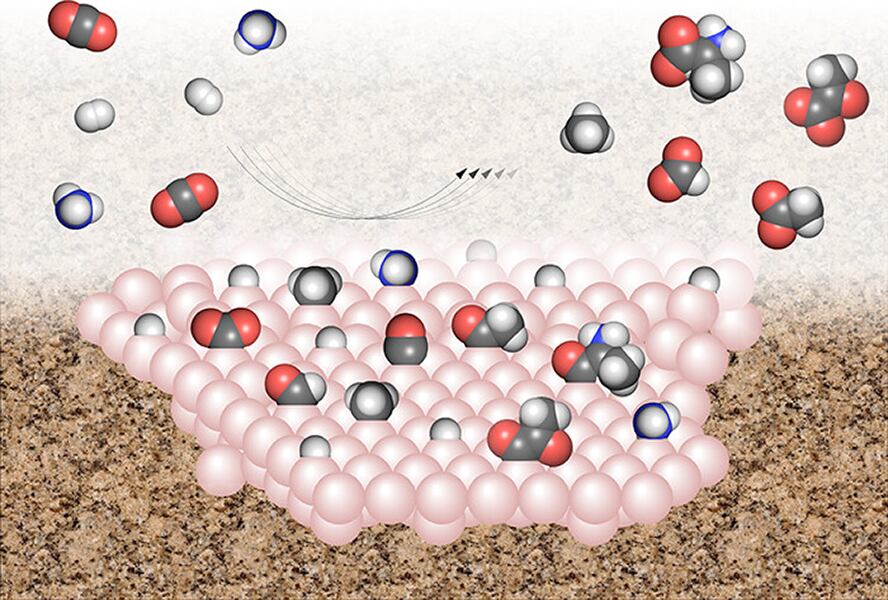
En otro informe, publicado en 2020, Preiner realizó pruebas en una serie de reactores químicos que soportaban altas temperaturas. En estos recipientes introdujo dióxido de carbono, así como viales que contenían agua más hierro o níquel en diversas proporciones. Los dejó reaccionar durante la noche.

Los reactores produjeron de forma fiable formiato, acetato, piruvato, metanol y metano.
“Estos metales sustituyen a 127 enzimas y nos dan cinco productos que son exactamente los productos de la vía biológica”, afirma Martin.
Los científicos señalan que el hierro y el níquel se encuentran en las fuentes hidrotermales de las profundidades marinas, donde podrían haber ayudado a dirigir las reacciones prebiológicas.
Además, estos metales todavía se encuentran en las partes de las enzimas modernas que catalizan la vía del acetil-CoA dentro de las células.
Los metales abundaban en el planeta primigenio. El hierro, en particular, estaba en todas partes, afirma Markus Ralser, investigador del metabolismo en Charité - Universitätsmedizin de Berlín.
LEA MÁS: Moléculas que se autoreplican aportan claves sobre el origen de la vida
Avanzando sin enzimas
El piruvato que Preiner, Martin y Moran fabricaron en sus experimentos es esencial para otra parte importante del metabolismo celular: la producción de aminoácidos y nucleótidos. Las células necesitan aminoácidos para unirse y formar proteínas, y necesitan nucleótidos para producir ADN y ARN.
La línea de montaje que fabrica estas sustancias se denomina ciclo del ácido tricarboxílico inverso, y el piruvato es uno de sus elementos clave.
Moran lleva años buscando replicar el ciclo del ácido tricarboxílico inverso fuera de las células.
El principal desafío era que, aunque las reacciones en el ciclo del ácido tricarboxílico inverso son teóricamente posibles, algunas de estas reacciones tardan muchísimo en iniciarse. Tienen una barrera de activación alta. ¿Sería posible superar estas barreras de activación sin enzimas?
A partir de 2015, Moran y su equipo estudiaron las 11 reacciones principales del ciclo del ácido tricarboxílico inverso, probando todos los catalizadores metálicos y no orgánicos que pudieron conseguir en todas las condiciones imaginables: a diferentes temperaturas y valores de pH, en presencia de diferentes metales y minerales.
Algunos tubos de ensayo intentarían completar el primer paso: la conversión de piruvato en oxaloacetato. Otros intentarían llevar a cabo la siguiente reacción, de oxaloacetato a malato. Además de las reacciones centrales en el ciclo del ácido tricarboxílico inverso, los científicos investigaron las reacciones que se ramifican a partir de este ciclo para producir nucleótidos, aminoácidos y fosfatos de azúcar.
En 2019, el equipo de Moran dio a conocer que podían producir nueve de los 11 metabolitos del ciclo del ácido tricarboxílico inverso sin enzimas. También identificaron las condiciones en las que seis de las 11 reacciones pueden funcionar juntas, en el mismo tubo de ensayo.
“La gran mayoría de las reacciones y el metabolismo parecían lo suficientemente fáciles como para que pudieran producirse sin enzimas”, afirma Moran.
LEA MÁS: Nanocristales dan pista sobre origen de la vida en la Tierra
Pequeñas, pero cruciales piezas que faltan
Mientras continúan su trabajo sobre el inicio de la química de la vida, Preiner y Moran se han centrado en pequeños productos químicos llamados cofactores o coenzimas, que ayudan en las reacciones enzimáticas.
Los cofactores son extremadamente importantes.
“Realizan tareas bastante simples, pero muy, muy importantes del metabolismo”, dice Preiner. “Es difícil imaginar que ellos o algún químico como ellos no estuvieran involucrados desde el principio”.
Los científicos quieren saber el papel de estos cofactores en los albores de la vida y cómo se integraron en la geoquímica y posteriormente en la bioquímica.
Están descubriendo que los cofactores actuales pueden tener actividad catalítica, como una enzima. Algunos incluso pueden catalizar su propia producción. Por ello, tendría sentido, dice Moran, que estos cofactores hubieran sido cruciales para acelerar las reacciones metabólicas. Podrían haber acelerado algunas vías químicas sobre otras, ayudando a esculpir una red bioquímica.
Los científicos también piensan que algunos cofactores participaron en un paso fundamental en la evolución celular: la aparición de los genes. Un cofactor llamado NADH consta de dos nucleótidos, los componentes básicos de los que están hechos el ARN y el ADN.
“Podría ser que estas moléculas, en una Tierra primitiva, se estuvieran produciendo en exceso. Y así se les asignaron diferentes tareas: algunas de ellas se incorporaron al ARN y otras al metabolismo”, afirma Preiner.
Los investigadores saben que nunca sabrán exactamente cómo surgió la vida: son como arqueólogos que intentan reconstruir el pasado profundo a partir de escasas reliquias desmoronadas.
Aun así, los científicos han demostrado que es posible crear un metabolismo no enzimático asombrosamente similar al de los microbios en las fuentes hidrotermales, proporcionando pruebas clave para una idea teórica centenaria sobre los orígenes de la vida.
Este artículo apareció originalmente en Knowable en español, una publicación sin ánimo de lucro dedicada a poner el conocimiento científico al alcance de todos. Suscríbase al boletín de Knowable en español.